Amedeo Avogadro
 |
| Lorenzo Romano Amedeo Carlo Avogadro, Conde de Quarequa e de Cerreto |
Conte di Quaregna e Ceretto
Biografia
✰ Nascimento: 9 de agosto de 1776
Local:Turim-Itália
† Falecimento: 9 de julho de 1856
Local :Turim-Itália.
É autor de um dos mais importantes princípios da química moderna, a hipótese hoje conhecida como lei de Avogadro.
A conseqüência mais importante da lei de Avogadro foi o estabelecimento da constante universalmente conhecida como número de Avogadro, cujo valor foi pela primeira vez determinado, com certa aproximação, em 1865.
O Número de Avogadro é o número de moléculas contidas em um mol de qualquer substância. Seu valor é 6,02252.1023, de acordo com pesquisas efetuadas em 1965, que demonstraram, ainda, que o valor anteriormente fixado por Millikan, 6,06.1023, não era bastante preciso.
O Volume de Avogadro é o volume ocupado por 1 mol de qualquer gás, nas condições normais de temperatura e pressão (273 K e 1 atm). Nessas condições, seu valor, calculado pelo físico austríaco Joseph Loschmidt (1821 – 1895), é 22,412 litros.
Vida Acadêmica
Seu pai, Conde Filippo Avogadro, foi um célebre advogado, sendo eleito presidente do
senado de Piemonte em 1779. Foi para a escola de Turim, seguir carreira de advogado eclesiástico. Formando-se em bacharel em 1792, com 16 anos. 4 anos depois defendeu seu doutorado. Mesmo tendo uma carreira de sucesso na advocacia (fora secretário da prefeitura de Eridano) Avogadro se interessava pelas Ciências Naturais. Ainda como secretário da cidade de Eridano, Avogadro começou a estudar Ciências por conta própria: Física e Química. Em 1809 passou a lecionar física no Realle Collegio de Varcelli.Em 1811 enunciou sua famosa hipótese: "Iguais volumes de quaisquer gases encerram o mesmo número de moléculas, quando medidos nas mesmas condições de temperatura e pressão". Os contemporâneos, notadamente Berzelius, recusaram-se a aceitá-la. Só em 1858, quando Cannizzaro, baseando-se nela, estabeleceu em definitivo a teoria atômico-molecular, é que a hipótese de Avogadro foi universalmente consagrada como lei. Em 1820 ingressa na Universidade de Turim como responsável pela cadeira de física. Por essa época escreveu vários trabalhos sobre questões de química e de física, grande parte dos quais foi publicada nos Atti dell'Academia dessa Scienze, em Turim. Depois de vários incidentes, retirou-se, em 1850, da universidade Trabalhou por 30 anos lá, período em que boa parte de sua obra foi publicada.
senado de Piemonte em 1779. Foi para a escola de Turim, seguir carreira de advogado eclesiástico. Formando-se em bacharel em 1792, com 16 anos. 4 anos depois defendeu seu doutorado. Mesmo tendo uma carreira de sucesso na advocacia (fora secretário da prefeitura de Eridano) Avogadro se interessava pelas Ciências Naturais. Ainda como secretário da cidade de Eridano, Avogadro começou a estudar Ciências por conta própria: Física e Química. Em 1809 passou a lecionar física no Realle Collegio de Varcelli.Em 1811 enunciou sua famosa hipótese: "Iguais volumes de quaisquer gases encerram o mesmo número de moléculas, quando medidos nas mesmas condições de temperatura e pressão". Os contemporâneos, notadamente Berzelius, recusaram-se a aceitá-la. Só em 1858, quando Cannizzaro, baseando-se nela, estabeleceu em definitivo a teoria atômico-molecular, é que a hipótese de Avogadro foi universalmente consagrada como lei. Em 1820 ingressa na Universidade de Turim como responsável pela cadeira de física. Por essa época escreveu vários trabalhos sobre questões de química e de física, grande parte dos quais foi publicada nos Atti dell'Academia dessa Scienze, em Turim. Depois de vários incidentes, retirou-se, em 1850, da universidade Trabalhou por 30 anos lá, período em que boa parte de sua obra foi publicada.
Costante de Avogadro
 |
| Número de Avogadro |
A constante de Avogadro, ou antigamente conhecida como número de Avogadro (em homenagem a Amedeo Avogadro), é uma constante física fundamental que representa um mol de entidades elementares (entidades elementares significando átomos, moléculas, íons, eletrons, outras partículas, ou grupos específicos de tais partículas).
Formalmente, a constante de Avogadro é definida como o número de átomos de carbono-12 em 12 gramas (0,012 kg) de carbono-12, o que é aproximadamente igual a 6,02 × 1023. Historicamente, o carbono-12 foi escolhido como substância de referência porque sua massa atômica podia ser medida de maneira bastante precisa.
Conhecendo-se a constante de Avogadro e a massa atômica de um elemento, é possível calcular a massa em gramas de um único átomo.
Mais Informações...
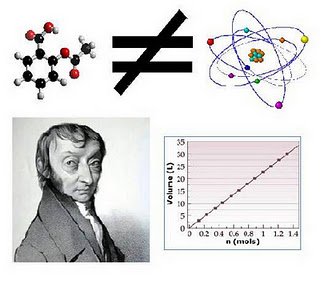 |
| Lei de Avogadro |
Conhecendo a constante de Avogadro e a massa atômica de um elemento, é possível calcular a massa em gramas de um único átomo.Avogadro tornou comum o uso da matemática em química, e pode ser considerado um dos fundadores da
Físico-Química.
Físico-Química.
Equipe:
Juliana Cajado nº 22
Sislana Azevedo nº38
Renata Bezerra nº 36
Maurício Torquato nº 34
Aymée Fontenele nº 06
Vinnya Freitas nº40
Bibliografias Consultadas
http://educacao.uol.com.br/biografias/amedeo-avogadro.jhtm
http://pt.wikipedia.org/wiki/Amedeo_Avogadro
http://allchemy.iq.usp.br/metabolizando/beta/01/avogadro.htm